 2024/11/13 10:36
2024/11/13 10:36
剑桥团队研发创新型神经袖套:一种微创周围神经接口技术
 2024/11/13 10:36
2024/11/13 10:36
周围神经接口技术在在慢性神经性疼痛、运动障碍、代谢性疾病及假肢的闭环控制等领域展现出巨大潜力。与非侵入性神经接口相比,植入式神经接口能够直接接触目标神经单元,实现精确的神经活动记录与调节。然而,传统神经袖套技术面临诸多挑战,包括植入手术复杂、设备刚性大、易导致神经损伤等问题,亟需创新突破。

近期,剑桥大学工程系研究团队开发出一种创新型的神经袖套。该神经袖套已通过动物实验验证,能在大鼠体内成功与坐骨神经形成稳定的生物电子接口,这显示其在微创术中实时神经监测和神经信号记录中的巨大潜力。这一突破性的软性电化学驱动技术将为神经系统疾病的诊断和治疗开辟全新路径,推动高精度、生物兼容的神经接口设备的广泛应用。
驱动器设计与制造
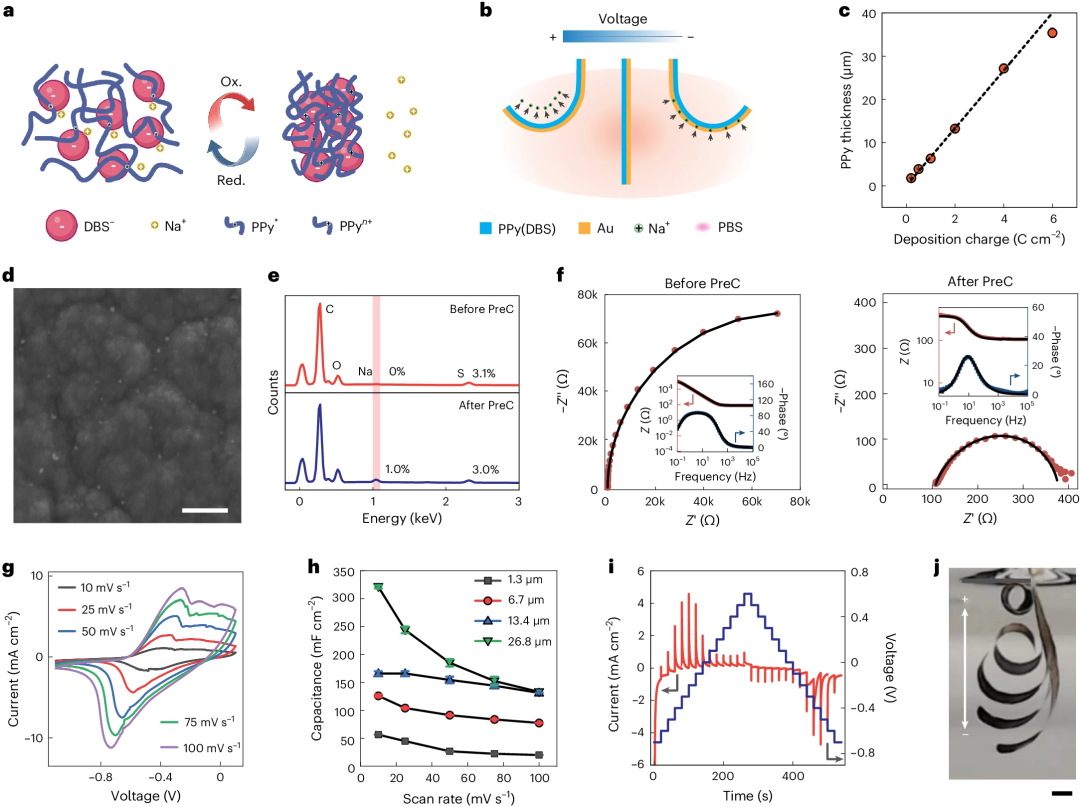
驱动器采用聚吡咯 (PPy(DBS)) 作为核心材料,凭借其在电化学刺激下的显著体积变化,能够实现精确的形态控制与功能优化。PPy(DBS) 材料的工作机制基于可逆电化学过程:负电压下,聚合物吸收溶剂化阳离子(如Na+),引发体积膨胀;正电压则导致阳离子排出,聚合物收缩(图 1a) 。研究团队通过电化学沉积技术,将PPy(DBS) 成功沉积在镀金的聚对二甲苯薄膜上,形成双层结构。这种结构展现出可控的弯曲能力(图 1b),实验结果表明其厚度与电荷量呈线性关系(图 1c),为未来设计提供了数据支持。
为确保驱动器的稳定性,研究人员采用循环伏安法对其进行预处理,激活材料的电化学性能。在几次扫描后,设备从平坦状态逐渐转变为卷曲形态。结果发现预处理后表面出现了纳米颗粒(图 1d),这表明材料内部发生了电荷转移与结构变化(图 1f)。进一步实验显示,驱动器在PBS溶液(生理相关环境)的电化学性能显著提升。见图1。
驱动器评估
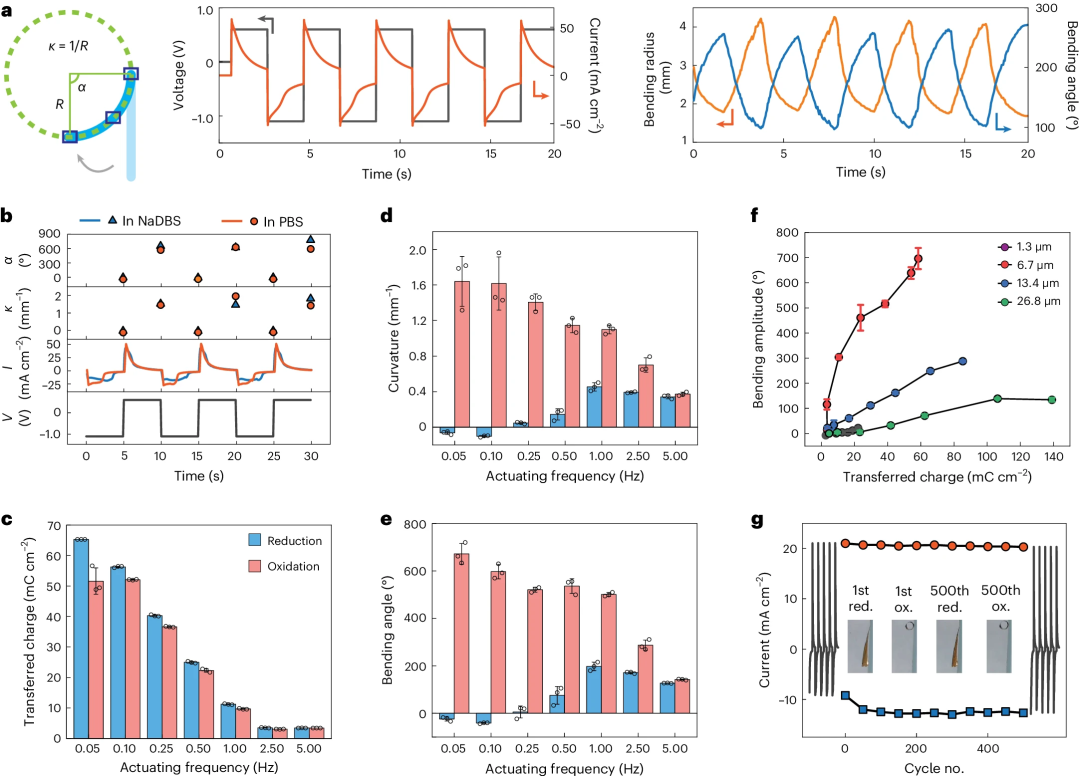
研究团队对基于导电聚合物的PPy(DBS)/Au/PaC驱动器进行了性能评估,驱动器以矩形结构为基础,采用运动学模型进行弯曲运动分析(图2a)。通过方波电压刺激,摄像机记录并结合计算机视觉技术分析其运动表现,评估参数包括弯曲角度、弯曲半径和曲率。结果显示,驱动器对电刺激响应迅速,并在反复刺激中保持高重复性和可逆性,性能表现稳定。
为了解驱动器在生理环境下的性能,研究人员进一步在PBS和NaDBS溶液中进行测试。在这两种溶液中,驱动器表现出显著的弯曲运动,甚至能够卷曲成螺旋形状,弯曲角度分别达到682°和597°(图2b)。在不同频率的方波电压下,驱动器的响应时间被量化分析,结果表明,随着频率增加,弯曲幅度逐渐降低,这是由于阳离子通过聚合物基质的时间所致(图2c-e)。此外,驱动器的弯曲幅度与PPy(DBS)薄膜的厚度密切相关,6.7 µm被确认为最佳厚度,实现了最大的弯曲幅度(图2f)。该研究还通过500次重复刺激循环验证了驱动器的稳定性和可靠性,展现了其在长期应用中的稳健性能(图2g)。
神经袖套电极的设计
神经袖套设计通过柔和抓握或螺旋缠绕方式紧密贴合神经,能够适应不同直径的神经,解决了传统袖套电极对齐不良的问题,大幅提升电信号传输的稳定性(图3a)。核心创新在于驱动元件与微电极阵列的无缝集成,利用光刻工艺确保其高效性和灵活性。例如垂直对齐的驱动元件设计允许设备沿电极方向大幅度弯曲,最小弯曲半径可达170微米(图3b)。通过不对称分布的驱动元件,袖套可在2.1秒内快速转变为螺旋形态,增强了适应不同神经形态的能力(图3c)。袖套整体结构精简,降低了机械不匹配风险,推动了设备的小型化与柔性化。静态拉伸测试显示其模量与PaC相似,展现出优异的柔韧性,有效减少植入物对神经组织的损伤。见图3.
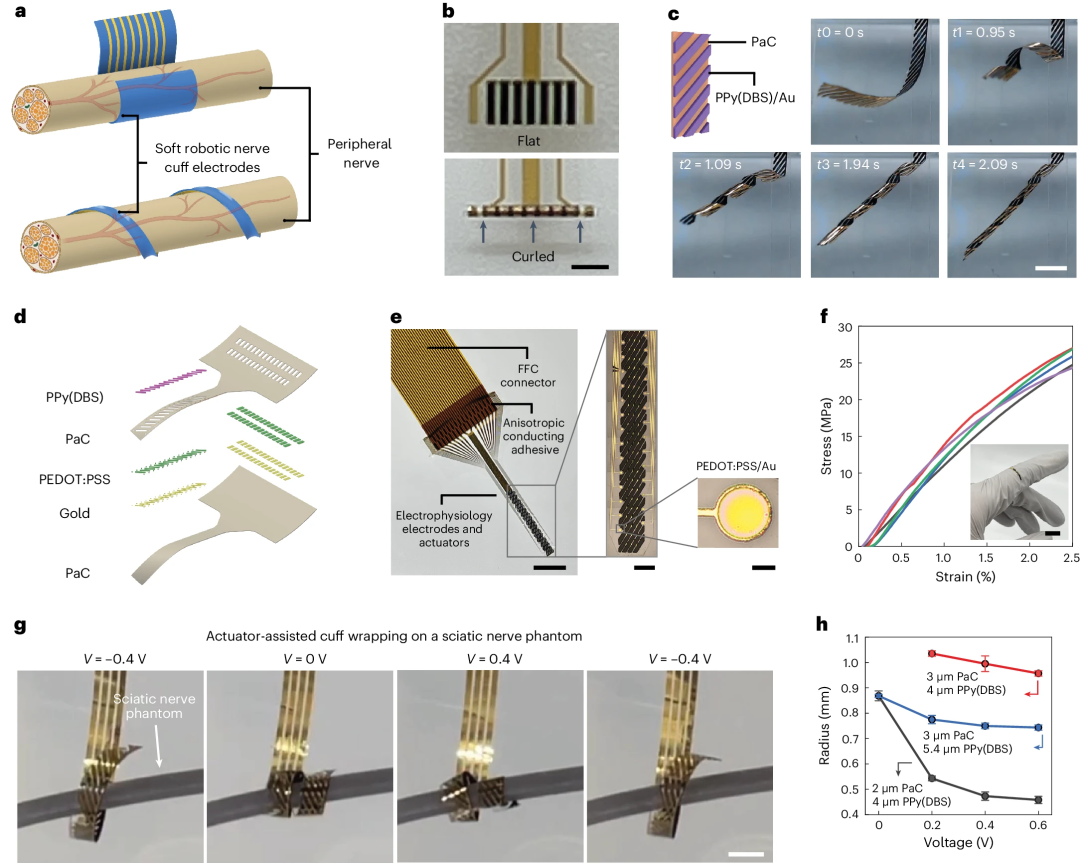
Fig3. 集成软执行器的神经袖带电极。a. 神经袖套示例。b. 光学显微镜照片显示了一种可弯曲成170微米弯曲半径的平坦袖套设备。c. 照片展示通过不对称图案驱动元件设计实现的2.1秒内螺旋路径快速驱动。d. 机器薄膜神经袖套每一层的爆炸渲染图。e. 与平坦柔性电缆(FFC)连接器粘接的设备照片。f. 由1.95微米PaC、10纳米Ti、100纳米Au和6.70微米PPy(DBS)组成的薄膜设备的应力-应变曲线。g. 神经袖套在PBS中的1.4毫米神经模型上缠绕的过程。h. 比较不同电压下螺旋结构的半径,测量了不同厚度的PaC和PPy样品。
神经袖套的在体验证
随后,研究人员在大鼠体内进行神经袖套的在体验证。厚度为2微米的PaC和4微米的PPy(DBS)组合的神经袖套,集成了28个聚(3,4-乙二氧噻吩)聚苯乙烯磺酸盐(PEDOT:PSS)/Au微电极,用于大鼠坐骨神经位置记录神经活动。实验结果表明,该设备能够与神经形成稳定的接口(图4a-c)。
研究人员将袖套电极放置于麻醉大鼠的坐骨神经上。通过控制施加电压,设备能够灵活调整其形状,从螺旋缠绕状态转换为贴合神经的界面,实现了多次调整以确保最佳的电接触。此过程无需使用任何固定胶水或缝线,展现出极高的操作简便性和生物兼容性。结果发现,神经袖套成功捕捉到与刺激相关的脉冲信号,信号质量稳定且基线噪声较低(图4e-g)。
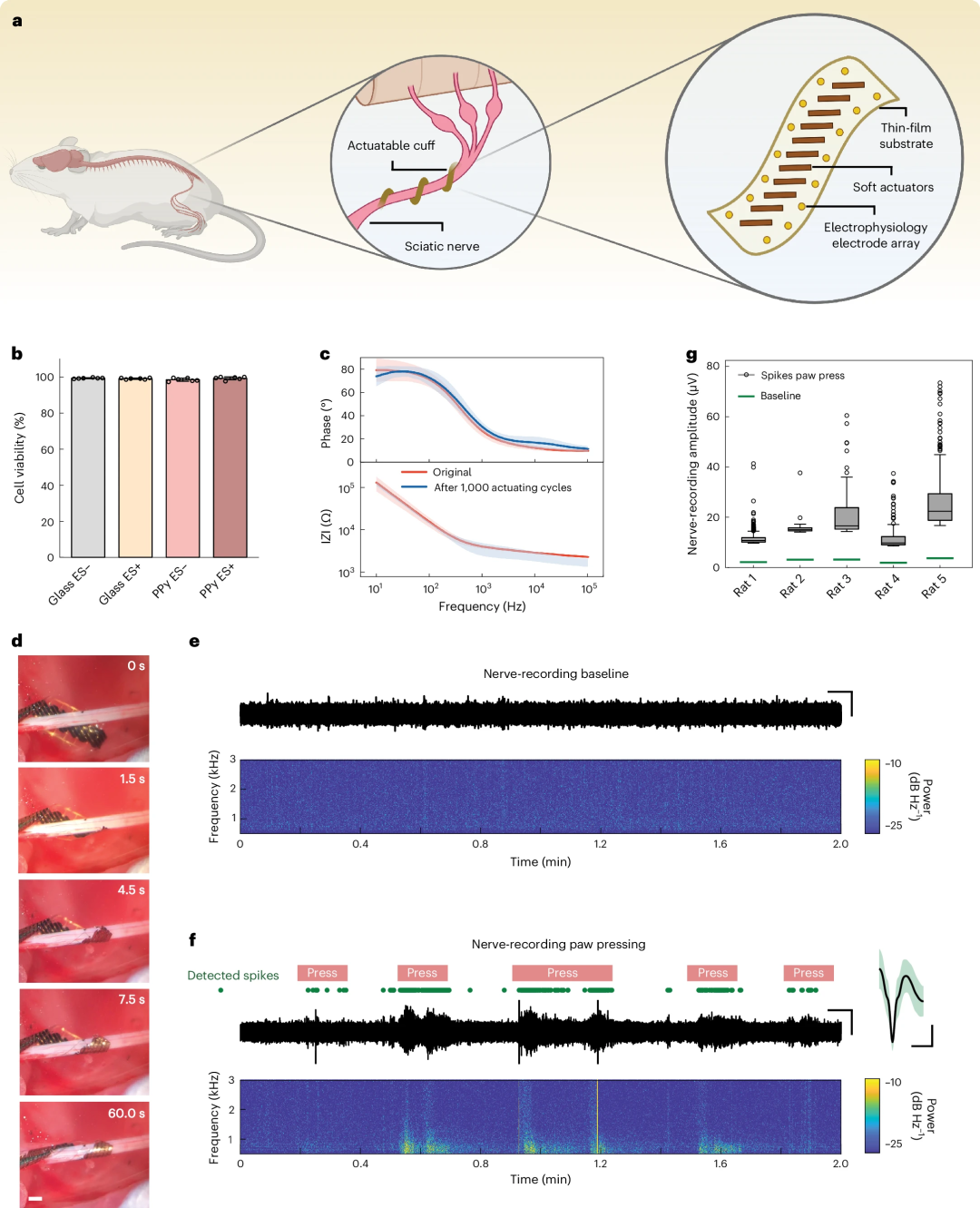
Fig4. 用于微创手术的软推杆辅助周围神经袖带的植入和活体验证。a. 灵活神经袖套概念示意图。b. 聚吡咯PPy(DBS)和对照组玻璃片的细胞活力分析。c. 神经记录微电极在1,000次驱动循环前后的电化学阻抗幅值(下)和相位(上)。d. 神经袖套在电压从-0.5V切换到0V时自缠绕在坐骨神经上。e. 记录植入麻醉大鼠坐骨神经的软体驱动袖套电极的基线噪声。f. 感觉刺激时的坐骨神经活动。g. 通过按压爪子对五只大鼠的五个植入驱动袖套记录到的脉冲噪声(绿色线)和脉冲幅度(箱线图)的量化结果。
结论
剑桥大学研究团队创新性地开发出一种柔性、低电压驱动的神经袖套电极,适用于微创神经接口手术。此种神经袖套集成精确图案化的驱动元件和微电极阵列,无需体积庞大的驱动器或复杂的控制系统,通过可逆的电压控制实现形状变化。在体动物实验发现,神经袖套实现了自缠绕神经,形成稳定接口,能够承受多次折叠和展开,且无额外固定操作。新型神经袖套有植入过程简单、良好的生物兼容性、设备易于移除、安全性高等优势。这一创新技术为神经系统疾病的诊断与治疗提供了全新的解决方案,推动了神经接口设备的发展。
仅用于学术分享,若侵权请留言,即时删侵!
本文来自新知号自媒体,不代表商业新知观点和立场。 若有侵权嫌疑,请联系商业新知平台管理员。 联系方式:system@shangyexinzhi.com